 El Instituto de Neurociencias, centro mixto del Consejo Superior de Investigaciones Científicas (CSIC) y la Universidad Miguel Hernández (UMH) de Elche, colabora en el primer ensayo clínico realizado en el mundo para probar si el medicamento defibrotide (DEF), ya autorizado para tratar una grave obstrucción de las venas sinusoidales hepáticas que en ocasiones sufren los trasplantados de médula ósea, sirve como terapia contra la enfermedad COVID-19.
El Instituto de Neurociencias, centro mixto del Consejo Superior de Investigaciones Científicas (CSIC) y la Universidad Miguel Hernández (UMH) de Elche, colabora en el primer ensayo clínico realizado en el mundo para probar si el medicamento defibrotide (DEF), ya autorizado para tratar una grave obstrucción de las venas sinusoidales hepáticas que en ocasiones sufren los trasplantados de médula ósea, sirve como terapia contra la enfermedad COVID-19.
El grupo de trabajo de Embiología Experimental del Instituto de Neurociencias, perteneciente a la Red Española de Terapia Celular (TerCel), trabaja en el desarrollo de experimentos que servirán para estudiar los efectos que el defibrotide tiene sobre las células del endotelio de los capilares sanguíneos del pulmón, y después sobre las células de los alveolos pulmonares.
El ensayo está coordinado por el Hospital Clínico Universitario Virgen de la Arrixaca (HCUVA) y el Instituto Murciano de Investigación Biosanitaria (IMIB). El Grupo de Trasplante Hematopoyético y Terapia Celular del IMIB, que dirige el Dr. José María Moraleda, presentó hace dos semanas esta propuesta a la convocatoria urgente del Fondo COVID-19, lanzada por el Instituto de Salud Carlos III (ISCIII) para la lucha científica y tecnológica contra la pandemia del coronavirus.
El ISCIII ha comunicado al IMIB la resolución favorable al estudio clínico propuesto por el Dr. Moraleda, en colaboración con un nutrido equipo multidisciplinar de clínicos e investigadores del Hospital Clínico Universitario Virgen de la Arrixaca, y de la Red Española de Terapia Celular (TerCel), concediéndole una dotación económica de 115.000 euros. El ISCIII considera que “la propuesta financiada resulta adecuada a la situación de emergencia, permitiendo una implementación y puesta en marcha inmediata en el Sistema Nacional de Salud, con resultados concretos, tempranos y oportunos a la situación actual”.
Autorización de la Agencia Española de Medicamentos
Como es preceptivo en este tipo de estudios, la Agencia Española de Medicamentos y Productos Sanitarios previamente ha emitido su resolución favorable al ensayo clínico al considerar que cumple con todos los requisitos de seguridad e idoneidad. Además, subraya que es “imprescindible trasladar lo más rápidamente posible a la práctica clínica la evidencia científica que generen las investigaciones sobre la COVID-19”.
“La idea partió de nuestro conocimiento del potente efecto antiinflamatorio y antitrombótico que el fármaco defibrotide logra en el tratamiento de la enfermedad veno-oclusiva hepática, que es una complicación muy grave que a veces sufren pacientes trasplantados de médula ósea, gracias a la protección del endotelio.
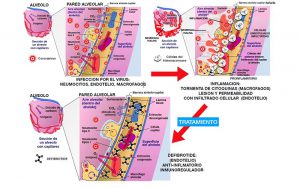
Ahí está la clave: el endotelio está formado por células que tapizan el interior de nuestras venas y arterias. El endotelio abre o cierra el paso de las células inflamatorias desde la sangre a los tejidos. Si protegemos el endotelio, evitaremos que las células inflamatorias del sistema inmune innato y adaptativo lleguen al pulmón en respuesta a la tormenta de citoquinas que provoca el virus y provoquen la inflamación masiva y el síndrome de distrés respiratorio característico de la COVID-19 y también las microtrombosis que causan el fallo multiorgánico y la muerte de estos pacientes”, explica el Dr. Moraleda, quien también dirige el Servicio de Hematología y Terapia Celular del HCUVA y es catedrático de Hematología de la Universidad de Murcia (UMU).
Primeros resultados en tres meses
El objetivo del ensayo es “demostrar que el defibrotide es eficaz y seguro como terapia contra la COVID-19 y estimamos que podría reducir en un 25% la tasa de mortalidad al lograr que los pacientes en estadios intermedios de la enfermedad no empeoren, evitando así la intubación. Y que los que ya están intubados, mejoren y se les pueda retirar la asistencia respiratoria mecánica”, añade el Dr. Moraleda.
Por ello, se reclutarán a 120 pacientes con diferentes grados de gravedad (intubados y no intubados) en el ensayo clínico aleatorizados en proporción 2:1; es decir, habrá 80 pacientes que recibirán el tratamiento experimental con defibrotide y otros 40 recibirán un placebo como grupo de control. Pero todos los pacientes podrán recibir todas las terapias que se están empleando actualmente para intentar frenar lainfección por SARS-COV-2, tales como antivirales, hidroxicloroquina, esteroides o tocilizumab, dado que el defibrotide no interacciona con ninguno de ellos y es
perfectamente compatible. Conviene resaltar que el defibrotide es un medicamento muy seguro, y en su indicación actual se puede utilizar en niños y lactantes a partir de un mes de edad.
Además de los pacientes que serán reclutados en el HCUVA, el ensayo contará con los diagnosticados que se recluten desde otros centros españoles: Fundación Jiménez Díaz y Hospital 12 de Octubre de Madrid, H. Clínic de Barcelona, H. U. de Salamanca, y H. U. Morales Meseguer.
Jazz Pharmaceuticals, la multinacional farmacéutica responsable del defibrotide, ha confirmado al equipo del IMIB que, apoyará la realización de este ensayo. El Dr Moraleda precisa que “la empresa se ha mostrado desde el primer momento muy comprometida con la investigación de fármacos ya disponibles como defibrotide, para combatir las graves consecuencias de esta enfermedad, lo que ha sido decisivo para que el estudio se pueda llevar a cabo.
El investigador principal del ensayo hace hincapié en que “estamos obsesionados con la calidad científica del ensayo en un momento de tanta incertidumbre terapéutica”. Este proyecto busca obtener evidencia científica, dar esperanza a los afectados basada en la eficacia comprobada del fármaco, no en la opinión sin contrastar de expertos con buena voluntad. Esperamos tener los primeros resultados en unos tres meses, con los análisis de los datos que nos ofrezca la aplicación de la terapia en los primeros pacientes. Vamos a empezar inmediatamente, porque “nuestros pacientes necesitan angustiosamente tratamientos eficaces con garantías científicas”. También indica que, paralelamente, se realizarán estudios biológicos para profundizar en el conocimiento
de la enfermedad y los efectos del tratamiento.
El Dr. Moraleda resalta el carácter multidisciplinar del ensayo y agradece el enorme esfuerzo y colaboración del equipo de Hematología y de todos los Servicios directamente implicados en su desarrollo como el Servicio de Medicina InternaInfecciosas, Cuidados Intensivos, Farmacia, Análisis clínicos, Inmunología, Radiología, Microbiología y Enfermería del Hospital Clínico Universitario de la Arrixaca; así como la eficiente gestión de la FFIS y la ayuda de los investigadores básicos del IMIB y de la Red de Terapia Celular (TerCel).
Colaboración internacional
Paralelamente al inicio del ensayo clínico en Murcia, el Dr. Moraleda destaca que ya se ha iniciado un grupo de trabajo con prestigiosos investigadores de instituciones internacionales para, en un futuro próximo, ampliar el ensayo clínico a otros países. En concreto, la colaboración internacional se está tramitando con el profesor Paul G. Richardson, profesor de Harvard Medical School y del Dana-Farber Cancer Institute (Boston, EE. UU.), el profesor Carmelo Carlo Stella, del Cancer Center HumanitasResearch Hospital (Milán, Italia), el profesor Favio Ciceri del Instituto San Rafaelle, (Milán, Italia), y el profesor Toni Pagliuca Kings Hospital (Londres, Reino Unido).
Fuente: CSIC
